11.8.2015 Anna Salonen
KEMIALLINEN REAKTIO
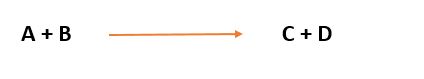
Lähtöaineet
A ja B reagoivat
muodostuu reaktiotuotteet C ja D. Nuolen päälle
usein kirjoitetaan olosuhteet, kuten käytetty lämpötila, paine tai katalyytti.
Lähtöaineiden A ja B kemialliset sidokset katkeavat ja järjestäytyvät uudelleen, jolloin muodostuu reaktiotuotteet C ja D.
Kemiallinen reaktio voi olla endoterminen (sitoo lämpöä) tai eksoterminen (vapauttaa lämpöä). Eksotermisestä reaktiosta esimerkkinä voidaan mainita polyesterikitin ja kovettajan välinen reaktio.
Jotkut reaktiot tapahtuvat helposti itsestään kun lähtöaineet yhdistetään. Toiset vaativat tiettyjä olosuhteita kuten esimerkiksi kuumentamista, katalyyttiä tai UV-valoa.
Kemiallisen reaktion nopeus riippuu
1. lämpötilasta. 2. Reagoivan aineen pinta-alasta 3. katalyytistä 4. reagoivan aineen luonteesta.
Esimerkkejä:
1. Ruoka pilaantuu kuumassa nopeammin kuin pakastimessa.
2. Jauhemainen sinkki reagoi suolahapossa palaa huomattavasti nopeammin.
3. Aine joka nopeuttaa reaktiota osallistumatta siihen itse (rikkihappo)
4. Epäorgaaniset aineet reagoivat tyypillisesti nopeammin kuin orgaaniset.
Hyvä esimerkkejä kemiallisesta reaktiosta ovat raudan ruostuminen, palaminen tai räjähdys.
Ruostumisessa rauta hapettuu ilman hapen ja kosteuden ansiosta, jolloin sen pintaan muodostuu huokoista rautaoksidia ELI RUOSTETTA. Kyseessä on raudan korroosio.
Lähtöaineiden A ja B kemialliset sidokset katkeavat ja järjestäytyvät uudelleen, jolloin muodostuu reaktiotuotteet C ja D.
Kemiallinen reaktio voi olla endoterminen (sitoo lämpöä) tai eksoterminen (vapauttaa lämpöä). Eksotermisestä reaktiosta esimerkkinä voidaan mainita polyesterikitin ja kovettajan välinen reaktio.
Jotkut reaktiot tapahtuvat helposti itsestään kun lähtöaineet yhdistetään. Toiset vaativat tiettyjä olosuhteita kuten esimerkiksi kuumentamista, katalyyttiä tai UV-valoa.
Kemiallisen reaktion nopeus riippuu
1. lämpötilasta. 2. Reagoivan aineen pinta-alasta 3. katalyytistä 4. reagoivan aineen luonteesta.
Esimerkkejä:
1. Ruoka pilaantuu kuumassa nopeammin kuin pakastimessa.
2. Jauhemainen sinkki reagoi suolahapossa palaa huomattavasti nopeammin.
3. Aine joka nopeuttaa reaktiota osallistumatta siihen itse (rikkihappo)
4. Epäorgaaniset aineet reagoivat tyypillisesti nopeammin kuin orgaaniset.
Hyvä esimerkkejä kemiallisesta reaktiosta ovat raudan ruostuminen, palaminen tai räjähdys.
Ruostumisessa rauta hapettuu ilman hapen ja kosteuden ansiosta, jolloin sen pintaan muodostuu huokoista rautaoksidia ELI RUOSTETTA. Kyseessä on raudan korroosio.